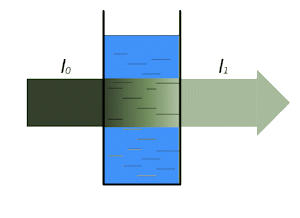
Oprócz jakościowego pomiaru absorpcji, który można w prosty sposób stwierdzić obserwując kolory zmianę światła przechodzącego przez badany obiekt, zjawisko absorpcji można opisać pewnymi regułami matematycznymi.
W spektrometrach, światło które przechodzi przez próbkę jest monochromatyczne. Oznacza to, że promieniowanie elektromagnetyczne posiada określoną długość fali, a nie jest mieszaniną fal o różnych długościach. Oprócz długości fali, inną ważną wartością dotyczącej wiązki promieniowania jest natężenie światła. Światło które pada na badaną substancję może z nią oddziaływać na cztery sposoby:
- Odbicie (Iodb)
- Rozproszenie (Iroz)
- Absorpcja (Iabs)
- Brak oddziaływania – promieniowanie przechodzi przez próbkę (I)
Oznacza to, że natężenie promieniowania można rozbić na cztery składowe:
I0=Iodb+Iroz+Iabs+I
W praktyce jednak wiązka światła wpada prostopadle do próbki, co powoduje że natężenie światła odbitego jest minimalne. Również ze względu na klarowność roztworów używanych w spektrometrii absorpcyjnych, natężenie promieniowania rozproszonego jest również niewielkie. Widać więc, że największy wkład do zmiany natężenia światła ma zjawisko pochłaniania. Pierwsze próby opisujące ilościowo prawo absorpcji zostały niezależnie opisane przez Bouguera w 1728 roku oraz przez Lamberta w 1760 roku. Założono wtedy, że światło przechodzi przez „cienkie” warstwy cząsteczek, które tak samo osłabiają wiązkę światła. Przyjmuje się wtedy, że każda warstwa jest taka sama, dlatego zamiast liczby cząsteczek podaje się długość drogi przez jaką promieniowanie przejdzie:
I0=exp(−kl)
Gdzie: k – współczynnik proporcjonalności, l – długość drogi optycznej
Prawo te, znane jest jako prawo Bouguera-Lamberta lub I prawo absorpcji promieniowania elektromagnetycznego. W roku 1820, prawo te zostało rozszerzone przez Beera. Innowacją było uwzględnienie różnych stężeń roztworów. Wprowadzono do wzoru współczynnik ekstynkcji oraz po przekształceniu wzorów wprowadzono wartość absorbancji. Tak zostało sformułowane prawo Bouguera-Lamberta-Beera, czyli II prawo absoprcji:
A=alc
Gdzie: A – absorbancja, a – współczynnik eksynkcji, l – długość drogi optycznej, c – stężenie roztworu
Dopełnieniem tych praw, jest III prawo absorpcji, która mówi o addytywności wartości absorbancji. Oznacza to, że jeżeli mamy oddzielnie różne mieszaniny o rożnych wartościach A, to mieszając je wszystkie, absorbancje jaką uzyskamy jest sumą wszystkich poszczególnych składników:
A=A1+A2+A3+…+An
Należy jednak pamiętać, że prawo to jest słuszne jedynie dla substancji, które nie oddziałują ze sobą.